做真题学化学-2023年新高考湖南化学卷第13、14题
做真题,学化学,带你畅游化学知识海洋,掌握化学内在逻辑规律,满分高分不是梦。第13题考查化学平衡及移动;第14题考查催化反应过程。13. 向一恒容密闭容器中加入1molCH4和一定量的H2O,发生反应:CH4(g) H2O(g)=CO(g) 3H2(g)。CH4的平衡转化率按不同投料比
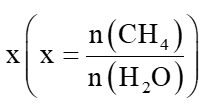
随温度的变化曲线如图所示。下列说法错误的是
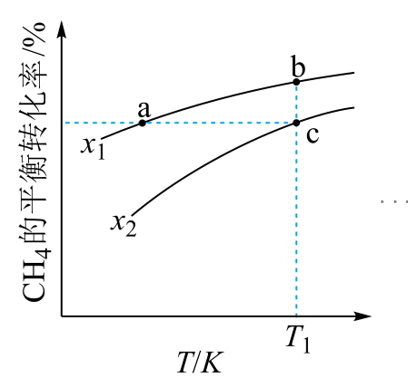
A. χ1<χ2B. 反应速率: Vb正<Vc正C. 点a、b、c对应的平衡常数:Ka<Kb=KcD. 反应温度为T1,当容器内压强不变时,反应达到平衡状态解析和解答如下:数据比较,需要控制变量。对选项A:比较x1和x2大小,选择温度均是T1时,此时平衡常数相同。通过平衡常数计算或勒厦特列原理,CH4的投料量为1mol,投料比x越大,投料n(H2O)越小,CH4的平衡转化率降低。x1<x2,正确。
对选项B:b、c两点处于平衡状态,正反应速率不好考虑,可以从逆反应速率入手。vb正=vb逆,vc正=vc逆,x1的平衡转化率高,生成的产物n(H2)、n(CO)多,浓度c(H2)、c(CO)高,vb逆>vc逆。错误。对选项C:x1和x2随温度变化趋势相同,选一条曲线分析温度的影响。温度升高,CH4的平衡转化率升高,平衡正向移动,平衡常数增大。反应为吸热反应。正确。
对选项D:该反应,为分子数增多的反应。反应未达到平衡时,气体物质的量在变,压强一直在变。当压强不变时,气体的物质的量不再变化,达到平衡。正确。正确答案选B。
14. N2H4是一种强还原性的高能物质,在航天、能源等领域有广泛应用。我国科学家合成的某Ru(Ⅱ)催化剂(用[L-Ru-NH3] 表示)能高效电催化氧化NH3合成N2H4,其反应机理如图所示。
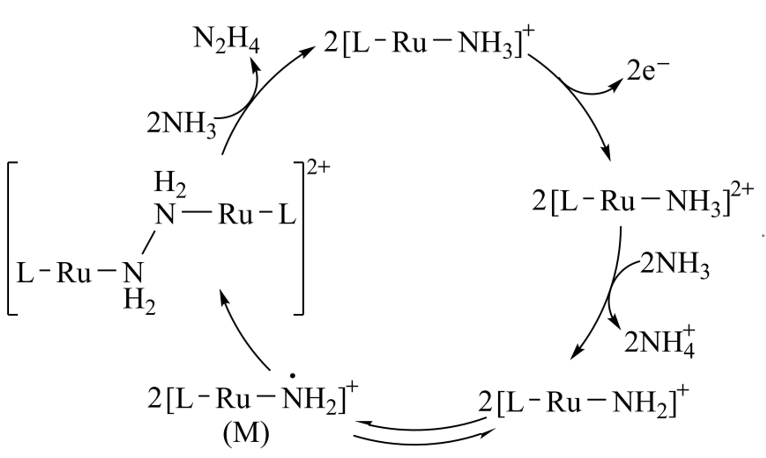
下列说法错误的是A. Ru(Ⅱ)被氧化至Ru(Ⅲ)后,配体NH3失去质子能力增强B. M中Ru的化合价为 3C. 该过程有非极性键的形成D. 该过程的总反应式:
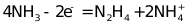
解析和解答如下:本题考查催化反应过程中电子、质子的转移、化合价。
[L-Ru-NH3] 失去1个电子,Ru(Ⅱ)被氧化为Ru(Ⅲ),变为[L-Ru-NH3]2 ,[L-Ru-NH3]2 与NH3反应,失去1个质子(H )变为[L-Ru-NH2] 。Ru(Ⅲ)的吸电子能力强于Ru(Ⅱ),配体NH3的N-H键极性增强,失去质子能力增强。选项A正确。[L-Ru-NH2] 到M,与外界没有电子转移,N上有一个单电子,只能是N的孤对电子拆分为2个,1个转移给了Ru(Ⅲ),Ru(Ⅲ)被还原为Ru(Ⅱ),另1个电子形成N上的单电子。选项B错误。对选项C:M中的2个单电子形成N-N共价键,由于M的对称性,形成的共价键为非极性键。正确。对选项D:观察反应过程中与外界的物质交换,方程式电荷守恒、原子守恒,正确。正确答案选B。微信号:麦爸说学习
- 0000
- 0000
- 0000
- 0000
- 0000